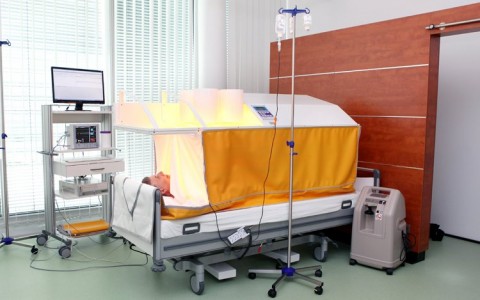
Uyarılmış tüm-vücut hipertermisi ilk olarak yirmi beş yıl önce hayvan deneklerde denenmiştir, ardından da son yirmi yıldır kanserli hastalarda ve sağlıklı gönüllüler üzerinde kullanılmaktadır. Ilk araştırmalarda terapiyi tatbik etmenin en etkin yolları, tedavi süresinin tanımlanması , ısı kaynakları , optimal sıcaklıklar ve oluşturulan etkiler bulunup çıkartıldı. Tedavi dendritik hücre aşılamaları gibi bağışıklık terapileri ve radyasyon , komoterapi ya da hormonlar gibi geleneksel terapilerle bir arada, bağımsız bir terapi olarak uygulandı. Onlarca yıllık araştırma, hiperterminin hastaların büyük çoğunluğu ve çoğu kanser türü açısından güvenli bir yöntem olduğunu gösterdi. Etkinlik. Katil (NK) hücreler kanser hücrelerinin yok edilmelerinde önemli bir rol oynarlar. Hipertermi NK hücrelerini harekete geçirmek için etkin bir uygulamadır. Dendritik hücreler aşılama vasıtasıyla uygulandığında, toksik (sitotoksik) T hücreleri vücuttaki kanser dokusuna karşı alarma geçirerek faal hale getirirler. Hep birlikte çalıştıklarında, bu bağışıklık hücrelerinin tümör gelişiminde engelleyici etkileri vardır.
Güvenlik ve Süre. 1980’li ve 1990’lı yıllarda yürütülen incelemeler hipertermiyi güvenli bir tedavi türü olarak belirlemiştir. Almanya’daki incelemeler de uygun ısı kaynağı olarak kullanılan infrared radyasyonun güvenliğini teyit etmiştir. Bu ateş-aralığı, tüm-beden hipertermisinde Medical Center Cologne’nda kullanılan ısıtma türüdür. Terapinin süresine gelince, daha önceki çalışmalar hipertermiyi otuz ila altmış dakika boyunca kullanmaktaydı, fakat günümüzde uygulanan çoğu tedavi, hastanın tepkisine bağlı olarak, genelde bir ila iki saat sürmektedir. Artı, bunu bir ila iki saatlik bir soğuma süresi takip eder. Gorter Modeli, sıcaklığın iki saat ya da daha uzun bir süreyle aşama aşama yükseltildiği, bunu normal sıcaklık elde edilene kadar yapılacak soğutma işleminden evvel sıcaklığın altmış dakika boyunca sabit tutulduğu (plato) bir zaman aralığının izlediği, en az üç ila dört saatlik bir protokolü takip eder.
İç Sıcaklığın Düşürülmesi. Araştırmalar, mineral banyoları ve jakuziler gibi geleneksel ısı terapisi türlerinin iç sıcaklık üzerinde çok sınırlı etkilerinin olduğunu tasdiklemiştir. Almanya, Hannover Tıp Okulu’nda yapılan bir araştırma, vücut sıcaklığının yavaş yavaş 42°C’ye kadar ısıtılan sıcak banyolarla artırıldığında, iç sıcaklığın esasen normalin 0.4°C üzerine çıktığını göstermiştir. Bağışıklık Sistemini Etkinleştirmek. Bağışıklık sisteminin 38.5°C’ye yükselterek kandaki bağışıklık faaliyeti seviyesini iki katına çıkarttığı ispatlanmış bir gerçektir. Bu yüzden, Köln Tıp Merkezi’nde hastalar üzerinde kullanılan maksimum sıcaklık 39°C’dir. Hipertermiye getirilen bu ılımlı yaklaşım, bağışıklık tepkisini etkin bir şekilde desteklerken güvenlik faktörünü de yükseltir. Viyana Üniversitesi tarafından gerçekleştirilen bir araştırma, bir test tüpü değerlendirmesinde, kanın 39°C’a ısıtılması durumunda, koruyucu monosit seviyesinin on katına çıktığını gösterdi. Aynı araştırmacılar bu yükselişi tetikleyen mekanizmalardan tekinin, bağışıklık tepkisinin harekete geçirilmesinde rol oynayan kandaki bir etmen olan ısı-şok proteinleri olduğunu da teyit etti.
Vücudun zihnini hafifçe tıklatmak. Hamburg, Almanya’da yapılan bir inceleme, vücut sıcaklığındaki artışın tek başına bağışıklık tepkisini otomatikman harekete geçirmediğini keşfetti. Bu incelemede, kanser hastalarının sıcaklıkları hipertermiyle yükseltildi ve sıcaklıklarını artırmak için ağır fiziksel egzersizlere katılan sağlıklı gönüllülerinkilerle kıyaslandı. Her ne kadar her iki grup da yüksek sıcaklıklara ulaşmış olsalar da, kanser hastalarında bağışıklık fonksiyonu güçlenirken sağlıklı gönüllülerde hiç bir şey olmadı. Kanser hastalarındaki desteklenmiş bağışıklık etmenleri, büyüme hormonunu ve NK hücreleri ile T hücrelerin endüksiyonunu içerdi.
Sıcaklığı azaltmak. Gorter Modeli’nin tam aksine, yapılan araştırmaların bir çoğu 41.8°C ila 42°C aralığında sıcaklıklar kullanırlar. Bazı incelemelerde ise hastalar bu yüksek sıcaklıklara dayanabilsinler diye anesteziyle uyuşturulur. Biz gereksiz anesteziden her zaman kaçınılması gerektiğine inanıyoruz çünkü yaşlı hastalarda Sundowner Sendromu adıyla anılan bir fenomen olan dermansızlığı yaratabiliyor. Ayrıca anestezi genelde bağışıklık baskılıyor.
Yan etkisiz tedavi. Almanya’da hiperterminin fibromiyalji hastalarındaki ağrı için kullanımına dair yapılan bir inceleme sonucun güvenli ve etkin olduğunu göstermiş, “69 katılımcıdan 14’ünde (20%) yan etki gözlemlendi ama hepsi de 20 dakikadan daha önce kayboldu,” yorumunu getirmiştir. İnceleme, standart multimodal rehabilitasyonla birleştirilen hiperterminin, yaşam kalitesini artırmanın yanı sıra ağrıyı kaydadeğer derecede azaltması yönünde, standart terapiye kıyasla çok daha etkin olduğunu göstermiştir Üzüntü ve endişenin en aza indirgenmesi. Buffalo, New York’daki Roswell Park Kanser Enstitütüsü araştırmacıları, ateş-aralığı, tüm-beden hipertermi tedavilerinin “iyi tolere edildiğini, kalple, karaciğerle, böbrekle ya da akciğerle ilgili hiç bir kötü olayla karşılaşılmadığını” belirtmektedirler. Ancak, geçmişlerinde kalp rahatsızlığı ya da beyin tümörü yaşamış hastaların dikkatle taranması gerekir. Köln Tıp Merkezi’nde, hastaların sadece yüzde 70’inin hipertermi uygulamasını almaya uygun olduğu kanaatine varılmıştır. Merkezde kullanılan ek güvenlik önlemleri, dehidratasyondan kaçınmak için elektrolit IV solüsyonunu ve kalp hızının sürekli olarak gözetim altında tutulmasını kapsar.
Geleneksel terapilerle birlikte kullanılan terapatik ateş. Hiperterminin uygulananradyasyon ve kemoterapinin uygulama başarısını artırdığı, ilaç tedavisinin etkinliğini geliştirdiği de ispatlanmıştır. Hollanda’daki tıp merkezinde yürütülen bir inceleme, hem hipertermi hem de radyasyon tedavisi alan 378 kanser hastasının gösterdiği gelişimi gözlem altına aldı. Sekiz yıl boyunca, hastaların yüzde 77’sinde olumlu tepki saptandı. Bu hastalığa özel beş yıl hayatta kalma oranı yüzde 47’ydi, ki bu kanser tedavisinde istisnai bir durumdur. Toksisite hastaların yüzde 12’si açısından büyük bir sorundu. Araştırmacılar, tanıya ek olarak, “hipertermi uygulanma sayısının olumlu sonucun prediktörü olduğu” kararına vardılar. Araştırmaların büyük çoğunluğunda, hastaların yüzde 50’sinden fazlasında istikrarlı bir tarapatik tepki gözlemlendi – genelde bunların yüzde 56 ila 80’i tedavi edildi. Hipertermi Avrupa çapında kabul edilmeye başlanıyor, Birleşik Devletler’de de Pennsylvania Üniversitesi ve Texas Üniversitesi gibi üniversite tıp merkezlerinde inceleme altında. Biz bu araştırmanın bir sonraki aşamasının, ameliyata alınamaz tümörleri olan ya da toksisitesi daha düşük bir tedavi almayı arzulayan hastalara bağımsız kanser tedavisi şeklinde uygulanabilecek hipertermiye odaklanacağını öngörüyoruz.


 English
English Deutsch
Deutsch Nederlands
Nederlands Russian
Russian Italiano
Italiano Français
Français Português
Português العربية
العربية